炎症性肠病(inflammatory bowel disease,IBD)涵盖了一系列涉及胃肠系统的持续性炎症性疾病,其特征为长期的间歇性缓解和发作。虽然IBD在西方国家的发病率趋于平稳,但仍超过0.3%,而在新兴工业化国家的发病率较低但迅速上升,这表明IBD已成为一种真正的全球性疾病。IBD的常见症状包括持续性腹泻、频繁的腹痛、直肠出血和疲劳,这些症状严重降低了患者的生活质量。此外,多种肠外炎症如皮肤、眼睛和关节,以及继发性并发症如狭窄、脓肿和与溃疡性结肠炎(ulcerative colitis,UC)相关结肠癌,会进一步恶化了IBD患者的生活质量。IBD包括两种亚型,UC和克罗恩病(Crohn’s disease,CD)。UC仅限于结肠,炎症主要存在于黏膜和黏膜下层,而CD则可影响消化道的任何部分,其特征为斑片状、透壁性炎症。通常,UC的发病率高于CD。尽管目前有一些治疗UC的方法,但存在疗效有限、副作用严重以及费用高等缺点,因此,迫切需要开发有效的替代治疗方法。
尽管UC的病因尚未完全阐明,但可能涉及遗传易感性、免疫反应紊乱、上皮屏障受损以及肠道菌群失调。因此,目前正在开发多种针对UC的新型疗法,并取得了令人鼓舞的进展,包括免疫细胞的“交通控制”、免疫信号阻断、上皮屏障修复以及补充有益微生物。其中,益生菌因其开发和生产成本低而受到研究人员的优先关注。食品级微生物鼠李糖乳杆菌(Lactobacillus rhamnosus)是潜在的益生菌候选物之一。例如,L. rhamnosus OLL2838可改善UC小鼠的肠道屏障功能障碍,而L. rhamnosus SHA113则能够重塑UC小鼠的肠道菌群结构和组成。
L. rhamnosus MP108分离自中国台湾省一名婴儿的粪便,毒理学研究表明其是安全的。此外,先前的研究显示,L. rhamnosus MP108能够有效缓解特应性皮炎。然而,尚不清楚L. rhamnosus MP108是否能够缓解UC。
江南大学食品学院李慧臻博士和杨波研究员等以UC小鼠为研究对象,评估了L. rhamnosus MP108对小鼠UC的缓解作用,并在多维度探讨了其潜在机制,发现L. rhamnosus MP108可能通过增强肠道屏障、抑制炎症和调节肠道微生物群缓解小鼠溃疡性结肠炎,这为乳酸菌(lactic acid bacteria,LAB)缓解UC的机制提供了有价值的见解。
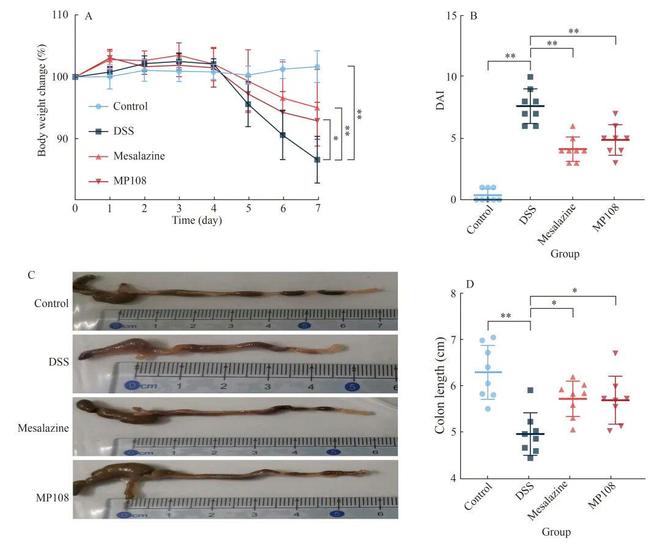
通过体重、DAI和结肠长度来研究L. rhamnosus MP108对UC症状的作用。与对照组相比,DSS导致小鼠体重显著降低、结肠显著缩短和疾病活动指数(disease activity index ,DAI)显著升高(图2)。然而,灌胃美沙拉嗪和L. rhamnosus MP108可显著抑制DSS引起的体重下降、DAI升高和结肠缩短。
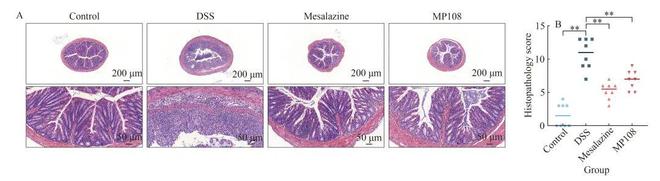
采用H&E染色观察结肠组织病理学变化。对照组小鼠结肠未见明显组织病理学异常。DSS组小鼠结肠出现大面积溃疡、黏膜上皮脱落、肠腺消失和炎症细胞浸润,导致DSS组的组织病理学评分显著高于对照组(图3)。同时,补充L. rhamno韦德国际最新官网sus MP108可减轻DSS引起的组织病理学损伤,并显著降低组织病理学评分,与美沙拉嗪组类似。
通过结肠切片的阿利新蓝染色和PAS染色以及结肠中的MUC2蛋白水平分析结肠黏膜屏障。与对照组相比,DSS导致小鼠结肠黏液减少、杯状细胞丢失和MUC2蛋白水平急剧降低;然而,美沙拉嗪和L. rhamnosus MP108干预显著抑制了上述不良变化(图4A-F)。通过测定血清 D-乳酸水平分析肠道通透性。有趣的是,美沙拉嗪和L. rhamnosus MP108干预显著抑制了DSS诱导的血清中D-乳酸水平升高(图4G)。对结肠切片进行TUNEL染色,以确定肠上皮细胞的凋亡情况。与对照组相比,DSS暴露小鼠的结肠上皮细胞凋亡增加,而美沙拉嗪或L. rhamnosus MP108干预可抑制这种凋亡(图5A)。利用结肠切片的透射电子显微镜图像揭示结肠上皮的超微结构。正常小鼠具有排列整齐的微绒毛 (microvilli,Mv),以及结构完整的紧密连接(tight junction,TJ)、黏附连接(adherens junction,AJ)和桥粒(desmosome,De韦德国际最新官网)(图5B)。DSS暴露的小鼠表现出Mv肿胀和排列紊乱,以及TJ、AJ和De模糊的结构。幸运的是,灌胃美沙拉嗪或L. rhamnosus MP108可显著阻止这些变化。总之,灌胃L. rhamnosus MP108可保护DSS暴露小鼠的结肠黏膜屏障。
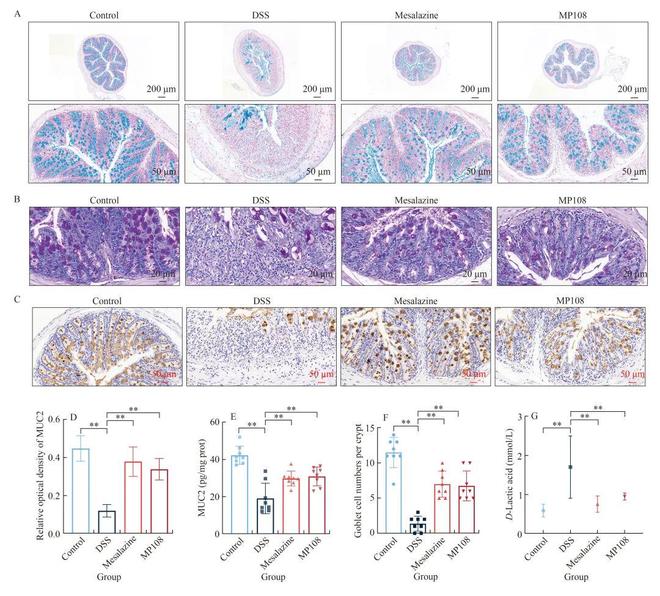
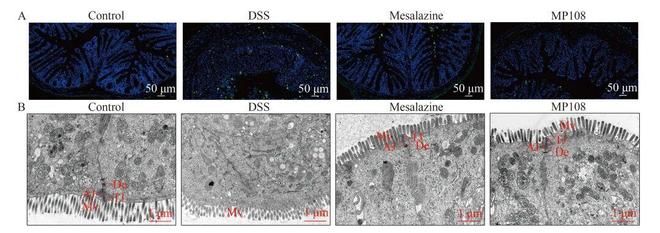
图5 L. rhamnosusMP108抑制结肠上皮细胞凋亡和结肠上皮结构破坏
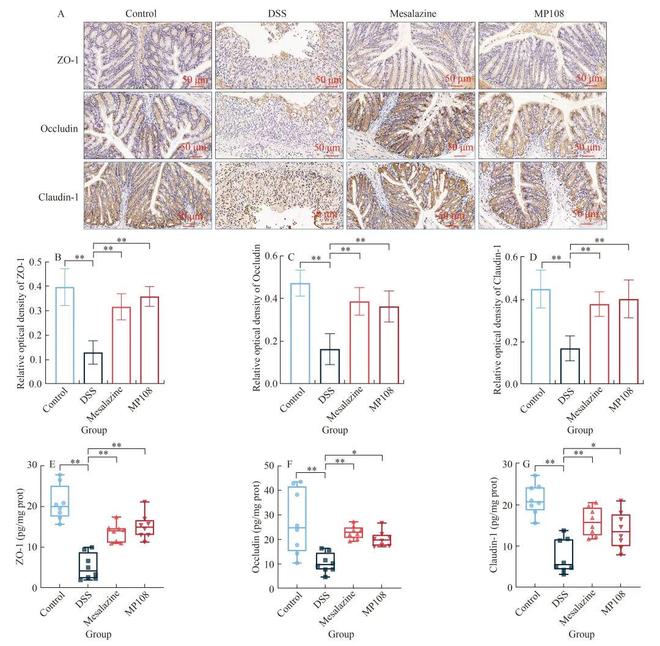
为了分析结肠中的TJ蛋白,作者对ZO-1、Occludin和Claudin-1进行了免疫组织化学(immunohistochemical,IHC)染色和ELISA测定。与对照组相比,DSS暴露小鼠的结肠中ZO-1、Occludin和Claudin-1的蛋白质水平显著降低,值得注意的是,灌胃美沙拉嗪或L. rhamnosus MP108显著提高了DSS暴露小鼠结肠中这3 种蛋白质的水平(图6)。
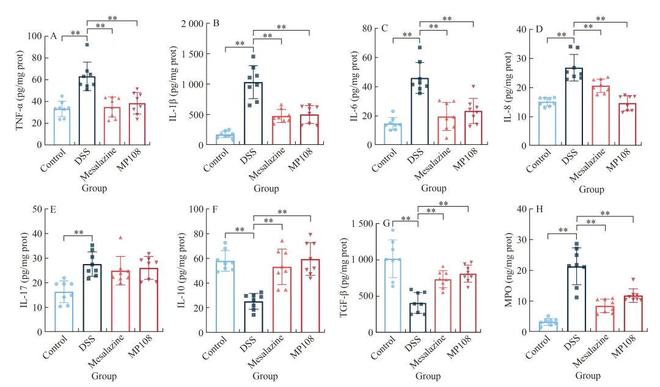
为了评估结肠炎症,使用ELISA检测结肠细胞因子和髓过氧化物酶(myeloperoxidase,MPO)水平。与正常小鼠相比,DSS导致结肠中TNF-α、IL-1β、IL-6、IL-8和IL-17的水平显著增加,IL-10和TGF-β的水平显著下降,而灌胃美沙拉嗪或L. rhamnosus MP108可显著抑制这些变化,但IL-17除外(图7A-G)。一致地,补充美沙拉嗪或L. rhamnosus MP108显著抑制DSS引起的结肠中MPO水平升高(图7H)。因此,这些结果表明,灌胃L. rhamnosus MP108可减轻DSS暴露小鼠的结肠炎症。
对于肠道菌群分析,对小鼠粪便进行了16S rDNA扩增子测序。四组共有74 个ASV,对照组和DSS组仅共有1 个ASV,而对照组和美沙拉嗪组共有7 个ASV,对照组和MP108组共有4 个ASV(图8A)。此外,对照组的独有ASV数量最多(28 个),其次是美沙拉嗪组(9 个)、MP108组(8 个)和DSS组(1 个)。
α-多样性以Chao1指数和Shannon指数表示。DSS组的Chao1指数和Shannon指数显著低于对照组(图8B-C)。然而,与DSS组相比,美沙拉嗪干预显著提高了Chao1指数,而MP108干预显著提高了 Chao1 指数和 Shannon 指数。
采用Bray-Curtis距离进行PCoA分析,且采用加权Unifrac距离进行聚类分析,以探究β-多样性。PCoA 图和聚类热图显示,与DSS组相比,美沙拉嗪组和MP108组更接近对照组。总之,L. rhamnosus MP108灌胃可改善DSS暴露小鼠的肠道菌群结构,使其与对照组相似。
图10 肠道菌群在属水平的共现网络模式以及差异细菌属与UC相关指标的相关性
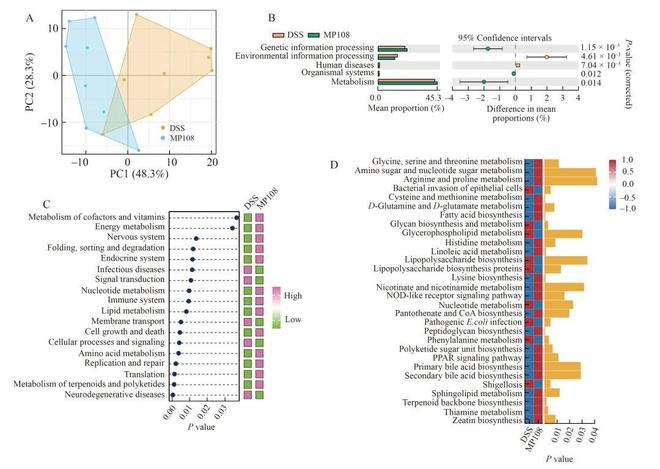
利用PICRUSt2预测了DSS和MP108组的肠道菌群功能。PCA揭示了DSS和MP108组肠道菌群功能的差异(图11A)。具体来说,在KEGG 1级通路中,与DSS组相比,L. rhamnosus MP108干预显著提高了与遗传信息处理以及生物体系统和代谢有关的基因比例,但显著降低了与环境信息处理和人类疾病有关的基因比例(图11B)。在KEGG 2级通路中,MP108组辅因子和维生素代谢、能量代谢、核苷酸代谢、免疫系统、脂质代谢、氨基酸代谢、复制和修复以及萜类和聚酮化合物代谢等基因含量显著高于DSS组,而传染病、细胞过程和信号传导以及神经退行性疾病等基因含量显著降低(图11C)。KEGG 3级通路分析显示,与DSS组相比,MP108组的氨基糖和核苷酸糖代谢、精氨酸和脯氨酸代谢、半胱氨酸和蛋氨酸代谢、脂肪酸生物合成、PPAR信号通路、初级胆汁酸生物合成、次级胆汁酸生物合成、鞘脂代谢以及硫胺素代谢相关基因的相对丰度显著升高,而与细菌侵袭上皮细胞、脂多糖生物合成、脂多糖生物合成蛋白和致病性大肠杆菌感染相关的基因的相对丰度显著降低(图11D)。总之,这些结果表明L. rhamnosus MP108治疗改善了UC小鼠的肠道菌群功能。
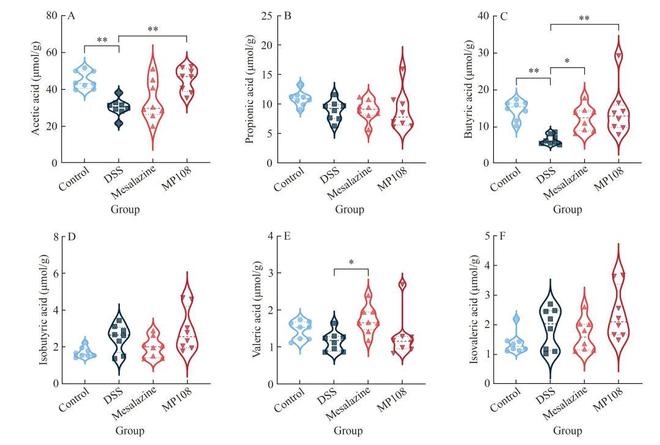
用GC-MS对盲肠SCFAs含量进行定量分析。与对照组相比,DSS暴露显著降低了乙酸和丁酸的含量(图12)。重要的是,与DSS组相比,美沙拉嗪组的丁酸和戊酸水平显著升高,而MP108组的乙酸和丁酸水平显著升高。
L. rhamnosusMP108可缓解DSS诱发的小鼠UC,其机制可能是通过增加MUC2的产生、抑制上皮细胞凋亡和防止细胞间连接破坏来增强肠道上皮屏障,维持促炎和抗炎细胞因子的平衡来抑制炎症以及调节肠道微生物群及其代谢物来促进肠道生态平衡。这项研究为揭示益生菌缓解UC的复杂机制提供了宝贵的线索,并为开发新的UC疗法或补充现有疗法提供了参考。


杨波,男,博士,研究员,博士生导师,无锡市预防医学会食品营养专业委员会副主任委员,江南大学母婴微生态与健康国际联合实验室负责人,食品生物技术中心-母婴童营养健康与乳品创新研究团队负责人。主要围绕母婴童微生态与健康调控、母婴童营养需求与特征解析、母婴童人群功能性食品、乳品营养与技术创新、母婴源益生菌及其活性代谢物的功能及应用展开。主持国家自然科学基金项目2项、国家十四五重点研发计划子课题1 项,参与国家自然基金重点项目等国家级项目5 项,主持产业化项目10余项。以第一/通信作者在Trends Microbiol、Trends Food Sci Tech、Prog Lipid Res、GutMicrobes、Crit Rev Food Sci、JAgric Food Chem、Food Funct和Appl Environ Microb等期刊发表SCI论文70余篇,获中国授权发明专利66余项。获教育部高等学校科学技术进步奖二等奖等省部级奖励3 项。担任《Frontiers in Microbiology》副编辑、《Microbiome Research Reports》青年编辑、《Annual Review of Food Science and Technology》客座编委和《iMeta》青年编委等职务。参与《乳酸菌科学与技术》(科学出版社)、《Lactic Acid Bacteria: Bioengineering and Industrial Applications》(Springer出版社)、《Bifidobacteria: Methods and Protocols》(Humana出版社)、《婴幼儿肠道菌群和益生菌新进展》(人民卫生出版社)等中英文专著的编写。
为汇聚全球智慧共探产业变革方向,搭建跨学科、跨国界的协同创新平台,由北京食品科学研究院、中国肉类食品综合研究中心、国家市场监督管理总局技术创新中心(动物替代蛋白)、中国食品杂志社《食品科学》杂志(EI收录)、中国食品杂志社《Food Science and Human Wellness》杂志(SCI收录)、中国食品杂志社《Journal of Future Foods》杂志(ESCI收录)主办,西南大学、 重庆市农业科学院、 重庆市农产品加工业技术创新联盟、重庆工商大学、 重庆三峡科技大学 、西华大学、成都大学、四川旅游学院、北京联合大学、 中国-匈牙利食品科学“一带一路”联合实验室(筹)、 普洱学院 共同主办 的“ 第三届大食物观·未来食品科技创新国际研讨会 ”, 将于2026年4月25-26日 (4月24日全天报到) 在中国 重庆召开。
为系统提升我国食品营养与安全的科技创新策源能力,加速科技成果向现实生产力转化,推动食品产业向绿色化、智能化、高端化转型升级,由北京食品科学研究院、中国食品杂志社《食品科学》杂志(EI收录)、中国食品杂志社《Food Science and Human Wellness》杂志(SCI收录)、中国食品杂志社《Journal of Future Foods》杂志(ESCI收录)主办,合肥工业大学、安徽农业大学、安徽省食品行业协会、安徽大学、合肥大学、合肥师范学院、北京工商大学、中国科技大学附属第一医院临床营养科、安徽粮食工程职业学院、安徽省农科院农产品加工研究所、安徽科技学院、皖西学院、黄山学院、滁州学院、蚌埠学院共同主办的“第六届食品科学与人类健康国际研讨会”,将于 2026年8月15-16日(8月14日全天报到)在中国 安徽 合肥召开。




